Para este contenido es necesario que conozcas y comprendas las características estructurales que tienen las principales moléculas existentes en los seres vivos, materia que puedes repasar revisando lo que estudiaste en primer año medio.
Veamos el siguiente ejercicio entregado por el DEMRE en 2010:
Los lípidos que constituyen las membranas de la célula se caracterizan por:
I) tener un extremo hidrofílico y otro hidrofóbico
II) ser insolubles en detergentes
III) ser apolares
Es (son) correcta(s)
A) sólo I
B) sólo II
C) sólo III
D) sólo I y II
E) sólo II y III
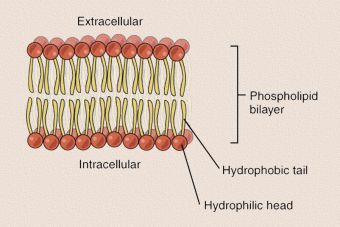
Lo primero es considerar que los lípidos constituyentes de las membranas celulares son esencialmente fosfolípidos, constituidos por una molécula de glicerol a la cual se esterifican en C1 y C2 dos cadenas de ácidos grasos, que componen la parte hidrofóbica de la molécula.
Por otra parte, en el C3 se une un grupo fosfato, cuyos oxígenos están cargados negativamente al pH celular, y al que podría unirse un alcohol polar que puede ser neutro o, de lo contrario, tener carga positiva o negativa.
Entonces, fosfato y alcohol constituyen el extremo hidrofílico de la molécula. Los fosfolípidos son, por lógica, moléculas anfipáticas, con un extremo hidrofóbico y otro hidrofílico. En consecuencia, lo que afirma I) es correcto.
Además, al entrar en contacto con el agua, las moléculas de fosfolípidos se organizan formando micelas o bicapas. En esas estructuras las cadenas hidrofóbicas de ácidos grasos se alínean unas con otras, interactuando entre ellas y dejando sus extremos hidrofílicos en contacto con el agua.
Estas estructuras son más o menos estables, pero posibles de romper si se utilizan compuestos de características similares a las de un fosfolípido; o sea, que tengan una parte hidrofílica y una hidrofóbica, como ocurre con los detergentes.
En solución acuosa, estos últimos rodean a las moléculas de fosfolípidos desestabilizando su organización: las cadenas hidrofóbicas quedan expuestas e interactúan con las cadenas hidrofóbicas del detergente; los extremos hidrofílicos de los fosfolípidos se ponen en contacto entre sí y los extremos hidrofílicos del detergente quedan expuestos al agua. Por ello es que los fosfolípidos son solubles en detergentes, lo que transforma a la opción II) en falsa.
Ahora, como vimos, la presencia de fosfato y de alcoholes polares genera que los fosfolípidos sean moléculas ligeramente polares, lo que inmediatamente nos hacer eliminar la afirmación III) como verdadera.
Por lo tanto, teniendo solo a la alternativa I) como correcta, nos encontramos con que la respuesta es A).
Para que continúes preparando tu PSU de Ciencias, recuerda ingresar a nuestro sitio. En él puedes revisar ejercicios sobre proporciones fenotípicas, Leyes de Newton y ondas electromagnéticas, entre otros contenidos.
Imagen CC Open Stax College